
Scopri come fattori ambientali, stress ossidativo, obesità, fumo, sonno e interferenti endocrini influenzano fertilità maschile e spermatogenesi.
Punti chiave dell’articolo
- La fertilità maschile dipende non solo dal numero di spermatozoi, ma anche dalla loro qualità, motilità e ambiente testicolare.
- Fattori ambientali come inquinamento, obesità e stress ossidativo influenzano negativamente la spermatogenesi e la qualità dello sperma.
- Gli interferenti endocrini e lo stress ossidativo danneggiano lo spermatozoo, compromettendo la fertilità maschile.
- Abitudini come fumo, alcol e uno stile di vita sedentario aggravano il rischio di infertilità; migliorare questi aspetti è cruciale.
- Mantenere un buon equilibrio tra salute generale, ambiente e stili di vita è fondamentale per la fertilità maschile.
La fertilità maschile non dipende soltanto dal numero di spermatozoi presenti nel liquido seminale. Oggi sappiamo che contano anche motilità, integrità del DNA spermatico, funzione mitocondriale, organizzazione della cromatina e qualità del microambiente testicolare [1,4,8,9].
Le evidenze più recenti indicano che fattori ambientali e stili di vita possono alterare la spermatogenesi attraverso meccanismi cellulari specifici, soprattutto stress ossidativo, infiammazione, alterazioni endocrine e danno epigenetico [1,2,3,5,7].
Indice
- Cos’è la spermatogenesi e perché è importante per la fertilità maschile
- Stress ossidativo e danno spermatico: il meccanismo chiave
- Inquinamento atmosferico e fertilità maschile
- Interferenti endocrini: cosa sono e come alterano la funzione testicolare
- Obesità, metabolismo e qualità dello sperma
- Fumo, alcol e abitudini che riducono la fertilità maschile
- Sonno, stress e ritmi biologici
- DNA spermatico ed epigenetica: perché oggi contano di più
- Come proteggere la fertilità maschile con lo stile di vita
- Conclusione
Cos’è la spermatogenesi e perché è importante per la fertilità maschile
La spermatogenesi è il processo con cui il testicolo produce spermatozoi maturi a partire dalle cellule germinali. Perché questo avvenga correttamente serve un equilibrio preciso tra cellule germinali, cellule del Sertoli, cellule di Leydig, segnali ormonali e assetto metabolico locale [4,8,9].
Quando questo equilibrio si altera, non si riduce solo la quantità di spermatozoi prodotti, ma può peggiorare anche la loro qualità biologica [4,8].
Le ricerche più recenti suggeriscono infatti che la fertilità maschile vada letta come il risultato di un ecosistema cellulare complesso. La funzione mitocondriale, l’organizzazione della cromatina spermatidica e i meccanismi epigenetici contribuiscono tutti alla capacità fecondante finale [4,8,9].
Per questo lo spermiogramma, pur restando fondamentale, non esaurisce da solo tutta la valutazione del potenziale riproduttivo maschile [8,9].
Stress ossidativo e danno spermatico: il meccanismo chiave
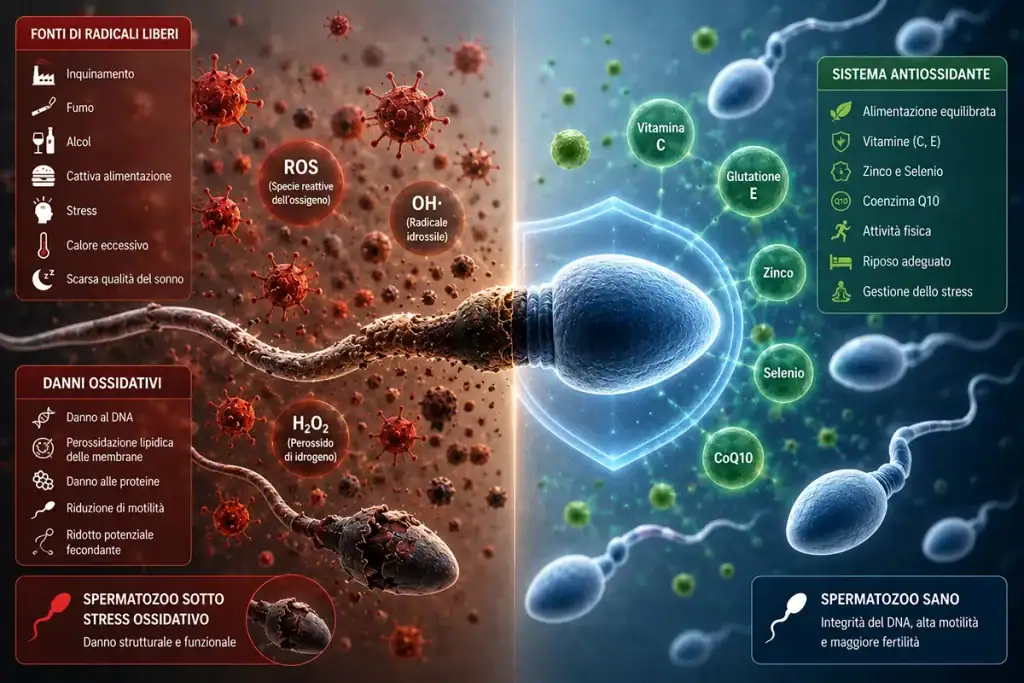
Tra i meccanismi che collegano ambiente, metabolismo e infertilità maschile, lo stress ossidativo è oggi considerato uno dei più rilevanti [2,5,6,7].
Si verifica quando la capacità antiossidante del sistema seminale e testicolare non è sufficiente a proteggere gli spermatozoi prodotti dal danno ossidativo [5,6].
In queste condizioni, gli spermatozoi diventano particolarmente vulnerabili perché possiedono membrane ricche di lipidi facilmente ossidabili con capacità riparative limitate [5,7].
Le conseguenze possono includere riduzione della motilità, danno delle membrane spermatiche, alterazioni mitocondriali e frammentazione del DNA spermatico [5,6,7].
Questo spiega perché fattori molto diversi tra loro — fumo, obesità, inquinamento, esposizioni tossiche e abitudini di vita scorrette — finiscano tutte insieme per convergere su questo danno finale comune [1,2,5,7].
Inquinamento atmosferico e fertilità maschile

L’inquinamento atmosferico è uno dei fattori ambientali oggi più studiati nel campo della fertilità maschile [2].
Le revisioni più recenti indicano che l’esposizione cronica a particolato sottile e ad altri inquinanti può associarsi a peggioramento della qualità spermatica, soprattutto attraverso aumento dello stress ossidativo e dell’infiammazione sistemica [2,10].
Il dato è rilevante perché suggerisce che l’ambiente non rappresenta un semplice sfondo, ma una componente attiva del rischio biologico.
Negli uomini che vivono in aree urbane ad alta esposizione, oppure che presentano già altri fattori predisponenti come sovrappeso, fumo o sedentarietà, l’inquinamento può contribuire in modo additivo al danno riproduttivo [1,2].
Interferenti endocrini: cosa sono e come alterano la funzione testicolare
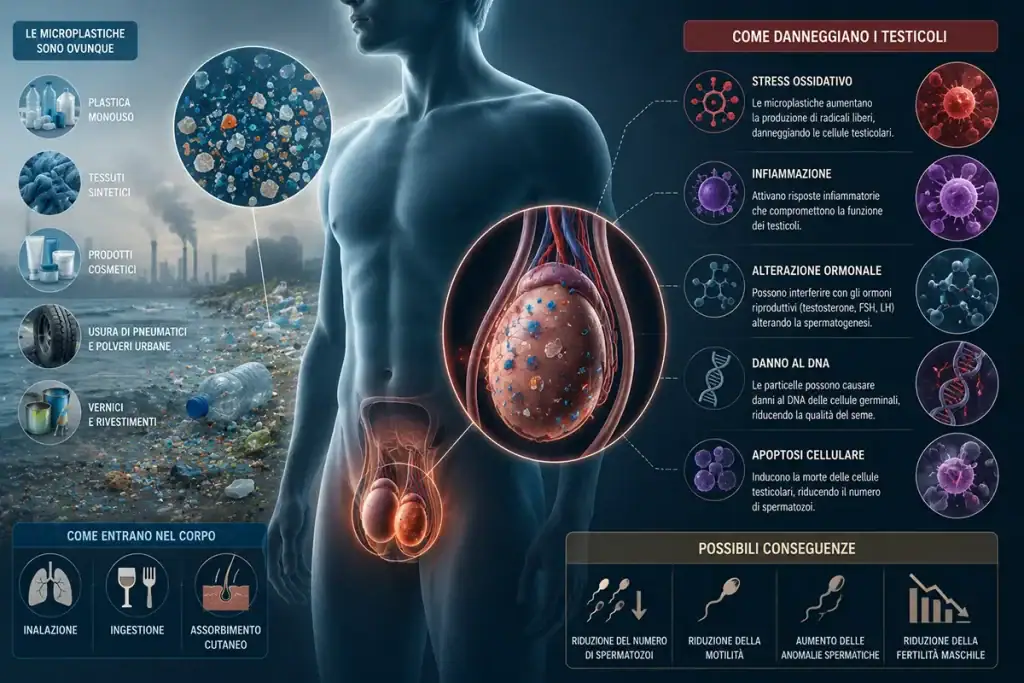
Tra i fattori ambientali più discussi rientrano gli interferenti endocrini, sostanze chimiche, naturali o sintetiche, in grado di alterare il normale funzionamento del sistema ormonale.
Fra queste sostanze troviamo bisfenoli, ftalati, pesticidi, PFAS e altri contaminanti emergenti [3,10,12]. Queste sostanze possono interferire con la normale segnalazione ormonale, alterare la steroidogenesi, favorire stress ossidativo e modificare l’assetto epigenetico delle cellule germinali [3,9].
Il problema non riguarda soltanto lo spermatozoo finale. Gli studi suggeriscono che gli interferenti endocrini possano colpire anche il microambiente testicolare, influenzando cellule del Sertoli e cellule di Leydig e destabilizzando così l’intero processo spermatogenetico [3,9].
Anche i dati recenti sulla presenza di microplastiche nel testicolo umano hanno rafforzato l’attenzione verso il ruolo dei contaminanti ambientali emergenti [10,12].
Obesità, metabolismo e qualità dello sperma
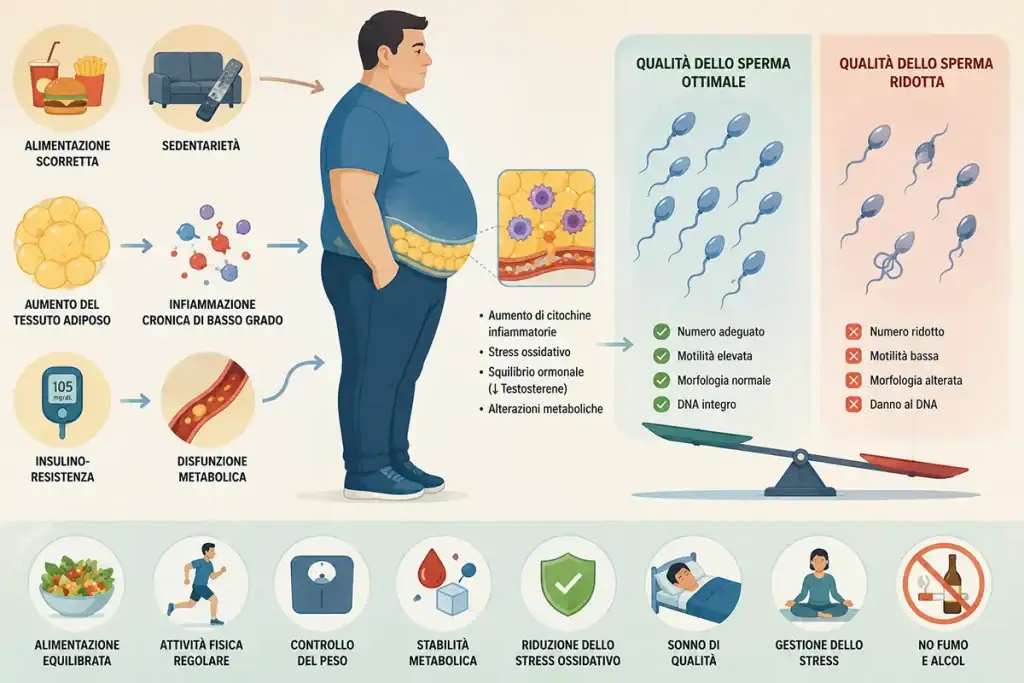
L’obesità è uno dei fattori modificabili più rilevanti che impattano sulla fertilità maschile [1,11].
Il tessuto adiposo in eccesso promuove infiammazione cronica di basso grado, insulino-resistenza, alterazioni ormonali e aumento dello stress ossidativo, tutti elementi che possono compromettere la spermatogenesi [7,11].
Dal punto di vista biologico, il danno può coinvolgere sia la produzione di testosterone sia il supporto metabolico e strutturale alle cellule germinali [11]. Inoltre, sovrappeso e sedentarietà possono associarsi a un peggioramento complessivo del contesto metabolico, con effetti sfavorevoli sulla qualità del seme [1,11].
Per questo la salute riproduttiva maschile è sempre più considerata strettamente legata alla salute cardio-metabolica generale [11].
Fumo, alcol e abitudini che riducono la fertilità maschile
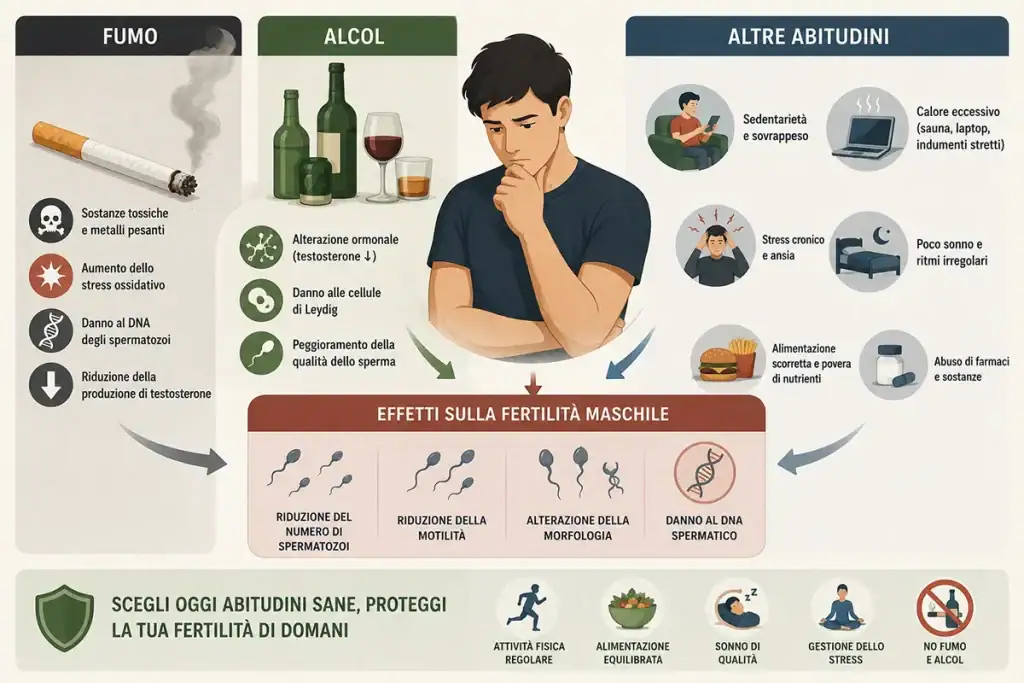
Il fumo di sigaretta è da tempo associato a peggioramento della qualità spermatica, soprattutto per il suo effetto sul danno ossidativo e sull’integrità del DNA spermatico [1,5,7]. Anche il consumo eccessivo di alcol può contribuire a uno squilibrio endocrino e metabolico sfavorevole [1].
L’aspetto più importante, però, è l’effetto cumulativo. Nella pratica clinica spesso non esiste un solo fattore dominante: fumo, scarsa qualità del sonno, stress, dieta inadeguata, eccesso ponderale e inattività fisica tendono a sommarsi lungo le stesse vie biologiche, cioè infiammazione, stress ossidativo e disfunzione endocrina [1,5,7].
È proprio questa convergenza che rende utile un approccio globale allo stile di vita.
Sonno, stress e ritmi biologici
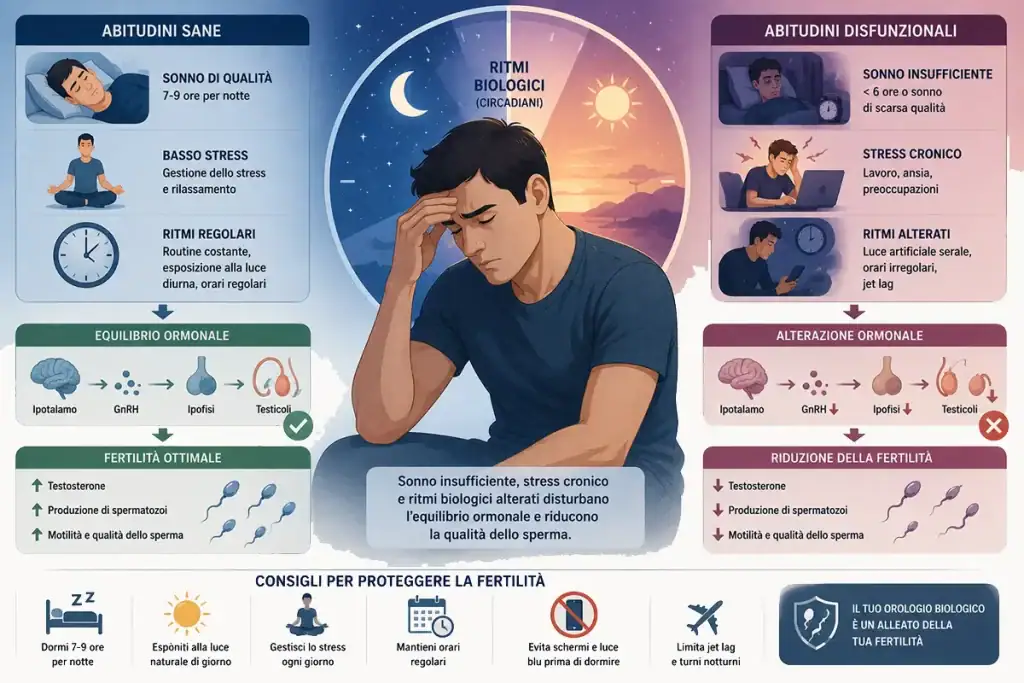
Anche il sonno e la regolazione complessiva dello stile di vita meritano attenzione.
Le sintesi più aggiornate sui fattori di rischio maschili includono il ruolo delle abitudini quotidiane e dei carichi cronici di stress tra gli elementi capaci di influenzare qualità spermatica e stato ossidativo [1,7].
In questo contesto, il sonno insufficiente e lo stress prolungato possono agire come amplificatori di infiammazione, disfunzione metabolica e abitudini sfavorevoli [1,7].
DNA spermatico ed epigenetica: perché oggi contano di più
Una delle novità più importanti della ricerca recente è l’attenzione crescente verso la qualità molecolare dello spermatozoo [3,8,9].
Sempre più studi sottolineano l’importanza della cromatina spermatidica, della frammentazione del DNA e delle modificazioni nella regolazione della espressione genetica come elementi capaci di influenzare fertilità, sviluppo embrionale e outcome riproduttivi [8,9].
Questo significa che uno spermatozoo può apparire quantitativamente adeguato ma presentare alterazioni molecolari che ne riducono la qualità biologica [8].
Gli interferenti endocrini e altri fattori ambientali possono agire proprio su questo livello, modificando l’assetto genetico delle cellule germinali [3,9].
Per questo la fertilità maschile viene oggi interpretata sempre meno come semplice conteggio di spermatozoi e sempre più come espressione di salute cellulare complessiva [4,8,9].
Come proteggere la fertilità maschile con lo stile di vita

Le evidenze disponibili non servono solo a descrivere il danno, ma anche a definire misure preventive realistiche.
Le strategie più sensate oggi includono controllo del peso, riduzione del fumo, moderazione dell’alcol, miglioramento complessivo dello stile di vita e, quando possibile, attenzione all’esposizione ambientale e professionale [1,2,7,11].
Questo approccio ha un razionale biologico forte. Intervenire su peso corporeo, abitudini tossiche e carico ossidativo significa agire direttamente sui meccanismi che la letteratura recente identifica come più rilevanti per la fertilità maschile [2,5,7,11].
In quest’ottica, la prevenzione preconcezionale nell’uomo dovrebbe essere considerata parte integrante della medicina riproduttiva.
Conclusione

Le nuove evidenze mostrano che la fertilità maschile è il risultato di un equilibrio fine tra spermatogenesi, metabolismo, ambiente e stile di vita [1,4,11].
Inquinamento, interferenti endocrini, microplastiche, obesità, fumo e danno ossidativo possono compromettere la qualità dello sperma attraverso vie biologiche convergenti [2,3,5,10,12].
Per questo la fertilità maschile va sempre più considerata come un indicatore della salute generale dell’uomo e del suo rapporto con l’ambiente [1,11].
In un’ottica clinica e preconcezionale, intervenire sugli stili di vita e limitare le esposizioni nocive non è un consiglio generico, ma una strategia con una base biologica concreta [1,2,7,11].
Bibliografia
[1] Sciorio R, Tramontano L, Adel M, Fleming S. Decrease in Sperm Parameters in the 21st Century: Obesity, Lifestyle, or Environmental Factors? An Updated Narrative Review. J Pers Med. 2024;14(2):198.
[2] Omolaoye TS, Skosana BT, Ferguson LM, Ramsunder Y, Ayad BM, Du Plessis SS. Implications of Exposure to Air Pollution on Male Reproduction: The Role of Oxidative Stress. Antioxidants (Basel). 2024;13(1):64.
[3] Deng X, Liang S, Tang Y, Li Y, Xu R, Luo L, et al. Adverse effects of bisphenol A and its analogues on male fertility: An epigenetic perspective. Environ Pollut. 2024;345:123393.
[4] Mai Z, Yang D, Wang D, Zhang J, Zhou Q, Han B, et al. A narrative review of mitochondrial dysfunction and male infertility. Transl Androl Urol. 2024;13(9):2134-2145.
[5] Pavuluri H, Bakhtiary Z, Panner Selvam MK, Hellstrom WJG. Oxidative Stress-Associated Male Infertility: Current Diagnostic and Therapeutic Approaches. Medicina (Kaunas). 2024;60(6):1008.
[6] Mottola F, Palmieri I, Carannante M, Rocco L. Oxidative Stress Biomarkers in Male Infertility: Established Methodologies and Future Perspectives. Genes (Basel). 2024;15(5):539.
[7] Sengupta P, Pinggera GM, Calogero AE, Agarwal A. Oxidative stress affects sperm health and fertility—Time to apply facts learned at the bench to help the patient: Lessons for busy clinicians. Reprod Med Biol. 2024;23(1).
[8] Balder P, Jones C, Coward K, Yeste M. Sperm chromatin: Evaluation, epigenetic signatures and relevance for embryo development and assisted reproductive technology outcomes. Eur J Cell Biol. 2024;103(3):151429.
[9] Hosseini M, Khalafiyan A, Zare M, Karimzadeh H, Bahrami B, Hammami B, et al. Sperm epigenetics and male infertility: unraveling the molecular puzzle. Hum Genomics. 2024;18(1):57.
[10] Daniels D, Berger Eberhardt A. Climate change, microplastics, and male infertility. Curr Opin Urol. 2024;34(5):366-370.
[11] Cannarella R, Crafa A, Curto R, Condorelli RA, La Vignera S, Calogero AE. Obesity and male fertility disorders. Mol Aspects Med. 2024;97:101273.
[12] Hu CJ, Garcia MA, Nihart A, Liu R, Yin L, Adolphi N, et al. Microplastic presence in dog and human testis and its potential association with sperm count and weights of testis and epididymis. Toxicol Sci. 2024;200(2):235-240.
Ti potrebbe interessare anche questo articolo



