Cistite ricorrente e cronica: anatomia della vescica, cause e fisiopatologia
Cistite ricorrente e cronica: anatomia della vescica, cause e fisiopatologia
La cistite ricorrente e la cistite cronica rappresentano una delle principali cause di infiammazione vescicale nella donna. Questa condizione è caratterizzata da dolore vescicale, urgenza urinaria e minzioni frequenti, spesso legate a una disfunzione della barriera uroteliale e alla perdita dei GAG vescicali.
Comprendere l’anatomia della vescica e i meccanismi fisiopatologici è fondamentale per impostare una corretta diagnosi e una efficace terapia della cistite cronica.
Anatomia della vescica
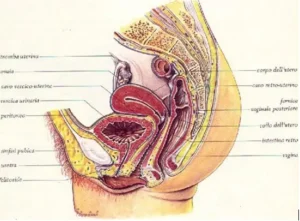
La vescica e l’uretra femminile sono alloggiate nel bacino e contraggono rapporti anatomici con:
- l’ampolla rettale posteriormente
- l’utero in sede postero-superiore
- la sinfisi pubica anteriormente
- la vagina anteriormente e inferiormente
Il peritoneo ricopre esclusivamente la parete superiore della vescica (cupola).
Le pareti vescicali sono costituite da tre strati:
- urotelio (strato mucoso interno)
- muscolo detrusore (strato muscolo-vascolare)
- pericistio (strato sieroso esterno)
Struttura interna della vescica
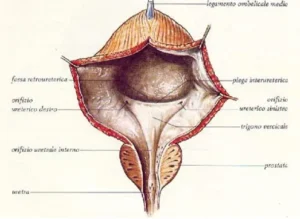
Macroscopicamente, la parete interna della vescica presenta il trigono vescicale, una regione triangolare dove sboccano:
- i due ureteri (trasporto dell’urina dai reni)
- il meato uretrale interno (deflusso urinario)
Innervazione vescicale e controllo della minzione
L’innervazione vescicale è costituita da vari sistemi: parasimpatico, simpatico e somatico.
Sistema parasimpatico (S2-S4)
- Contrae il detrusore
- Favorisce lo svuotamento vescicale
Sistema simpatico (D10-L2)
- Inibisce la contrazione
- Favorisce il riempimento
Sistema somatico (nervo pudendo)
- Controlla lo sfintere uretrale
- Garantisce la continenza urinaria
Le fibre afferenti trasmettono al cervello il senso di riempimento e gli stimoli dolorosi. Le fibre efferenti regolano la risposta motoria vescicale.
Questa complessa integrazione è alla base della fisiologia urinaria e della comparsa di ipersensibilità vescicale nei quadri patologici.
Fisiopatologia della cistite ricorrente e cronica
La cistite cronica è una patologia complessa caratterizzata da neuroinfiammazione vescicale e alterazioni della barriera uroteliale. Nella maggior parte dei casi, la prima manifestazione è una infezione batterica acuta, ma la cronicizzazione è legata a una disfunzione uroteliale persistente.
Approfondimento a cura de La Mia Ginecologa.
Fisiologia dell’innervazione vescicale
L’innervazione della vescica e degli organi pelvici deve rispondere alla necessità di integrare le funzioni urogenitali con la vita sociale. L’innervazione della vescica e degli organi sessuali parte dal lobo frontale per arrivare ai plessi pelvici. Affinché vi sia una situazione fisiologica i sistemi parasimpatico, simpatico e somatico devono continuamente interagire fra di loro.
Le fibre pregangliari parasimpatiche provocano la contrazione del detrusore e contemporaneamente il rilasciamento delle fibre del collo vescicale e dell’uretra. Originano a livello del secondo, terzo e quarto metamero sacrale (S2-S4). La loro origine così bassa spiega come anche in pazienti che hanno avuto lesioni totali midollari alte, alcune funzioni vescicali possano rimanere. Dalle aree di origine le fibre passano direttamente nel nervo pelvico il quale contrae rapporti anche con le fibre simpatiche.
Le fibre pregangliari simpatiche fondamentalmente inibiscono gli stimoli provocati dal parasimpatico. Originano a livello del decimo metamero dorsale fino al secondo metamero lombare (D10-L2). Da qui passano nei nervi lombari per arrivare al plesso ipogastrico che sia contrae rapporti con il plesso pelvico, sia arriva direttamente alla parete vescicale.
Le fibre somatiche conducono gli stimoli motori ai muscoli volontari del pavimento pelvico e di parte dell’uretra. Originano dal secondo, terzo, quarto metamero sacrale (S2-S4) e passano direttamente nel plesso pudendo e poi nel nervo pudendo. Inoltre un distinto nucleo motore (nucleo di Onuf), localizzato nel midollo anteriormente, fornisce fibre agli assoni che specificamente innervano lo sfintere uretrale esterno. Questo “super controllo” ci dimostra come la funzione della continenza urinaria sia così importante nella sua funzione psico-sociale.
L’innervazione nervosa della vescica è composta sia da fibre afferenti (che conducono messaggi dalla periferia al cervello), sia da fibre efferenti (messaggi mandati dal cervello alla vescica).
Al primo gruppo appartengono quelle fibre che portano in alto le sensazioni di riempimento vescicale generate sia dalla distensione passiva come dalla contrazione attiva. Esiste anche una seconda categoria di fibre, le cosiddette fibre silenziose o fibre C. Queste sono normalmente inattive, ma si attivano solamente in presenza di stimoli dolorosi o in presenza di calore. Ma la generazione dello stimolo nervoso avviene in vescica tramite l’attivazione dei recettori sensoriali che sono disposti nel contesto dell’urotelio e del detrusore.
E’ interessante segnalare anche l’unione che avviene fra le fibre di interesse prettamente vescicale e quelle mesenteriche e ipogastriche che innervano intestino e stomaco. Tale anastomosi spiega facilmente come stimoli dolorosi a partenza dalla vescica o dall’uretra possano coinvolgere anche l’intestino e lo stomaco.
Fisiopatologia della cistite ricorrente/cronica
Attualmente, nonostante la molteplicità delle ricerche, non si è completamente chiarita la cascata di eventi che porta allo stabilirsi della malattia cistitica cronica, mentre le molteplici strategie terapeutiche cosiddette sintomatiche, di solito falliscono o non hanno che un’efficacia di breve durata.
Nella maggior parte delle pazienti si può far risalire la prima manifestazione cistitica ad una infezione batterica acuta, anche se la quasi totalità dei ricercatori è concorde nell’affermare che questa condizione è probabilmente conseguente ad un difetto primario del rivestimento uroteliale.
Mentre nel passato si riteneva l’urotelio una semplice barriera, gli studi attuali ne hanno rivelato sia la sua funzione sensitiva, con la possibilità di informare il sistema nervoso centrale di stimoli termici, chimici o meccanici, che la sua attività efferente attraverso il rilascio di mediatori che influenzano la capacità contratturante delle cellule muscolari lisce della parete vescicale.
La capacità di tale barriera di mantenere integro il suo compito protettivo dipende dalla presenza dei GAGs (glucosamminoglicani) che ricoprono con uno strato “mucinoso” le sue cellule più superficiali.
Ruolo dei GAG e della barriera uroteliale
L’urotelio non è una semplice barriera, ma una struttura attiva con funzioni sensoriali, protettive e regolatorie.
I GAG vescicali formano uno strato mucinoso che:
- impedisce l’adesione batterica
- protegge da sostanze irritanti
- mantiene l’integrità della mucosa
La loro alterazione favorisce:
- infiammazione vescicale cronica
- infezioni urinarie recidivanti
- aumento della permeabilità uroteliale
Le cause che possono provocare la diminuzione o la perdita dei GAGs sono molteplici. Sicuramente un ruolo importante giocano le infezioni croniche ripetute, ma anche sostanze particolarmente aggressive o chemioterapici o radiazioni ionizzanti. Ricerche recenti hanno messo in luce, in pazienti allergiche al Nickel, la possibile diminuzione delle difese vescicali, con aumento di infezioni urinarie.
Infiammazione e neuroinfiammazione vescicale
Quando la barriera uroteliale è danneggiata, sostanze tossiche urinarie penetrano nei tessuti e si attivano mediatori come sostanza P, bradichinina e neurochinine.
Questi determinano:
- dolore vescicale
- contrazione del detrusore
- urgenza urinaria
Si instaura così un circolo vizioso tipico della sindrome della vescica dolorosa. Tutti questi meccanismi provocano l’istaurarsi della nevrite cronica con coinvolgimento neurologico e centrale.
La stimolazione cronica induce modificazioni a livello del midollo spinale:
- aumento delle sinapsi
- amplificazione del segnale doloroso
Si sviluppa così una memoria del dolore indipendente dallo stimolo periferico. Ad esempio la fisiologica sensazione di riempimento vescicale si trasforma in una sensazione di dolore urente, anche intensissimo, che costringe la paziente a minzioni frequentissime che a loro volta sono causa di ulteriore infiammazione.
Se questi segnali si ripetono continuamente, come accade nel dolore cronico, il sistema limbico (la centrale di gestione delle emozioni) provocherà prima manifestazioni di ansia e poi, al permanere del dolore, manifestazioni di angoscia fino al panico. A questo punto talvolta si potranno manifestare cambiamenti radicali dell’umore fino ad uno stato di depressione continua.
Ricerche sugli animali e sull’uomo hanno dimostrato che in fase depressiva la sensibilità al dolore aumenta, con conseguente abbassamento della soglia del dolore. La paziente allora metterà al centro della sua vita l’attenzione spasmodica continua ai suoi sintomi. Infatti, quando il dolore diventa neuropatico, l’attenzione allo stesso ne è una componente fondamentale. Ecco perché questo tipo di dolori diminuisce durante la notte per aumentare invece quando l’attenzione non è rivolta ad altri impegni importanti (es. nei fine settimana o in vacanza).




